抗体药物命名规则解析(2017年4月版)
近年来,治疗性抗体药物快速发展,抗体产品纷纷上市。
但是看着那些名字,是否感觉很难念,很难记?
是否好奇这些名字是怎么出来的,怎么命名的人脑洞如此大,能够想出如此稀奇古怪的名称?
在这里,我们就来简单回顾下这些命名规则,看完之后你会知道原来名字里面也隐藏了很多的信息。
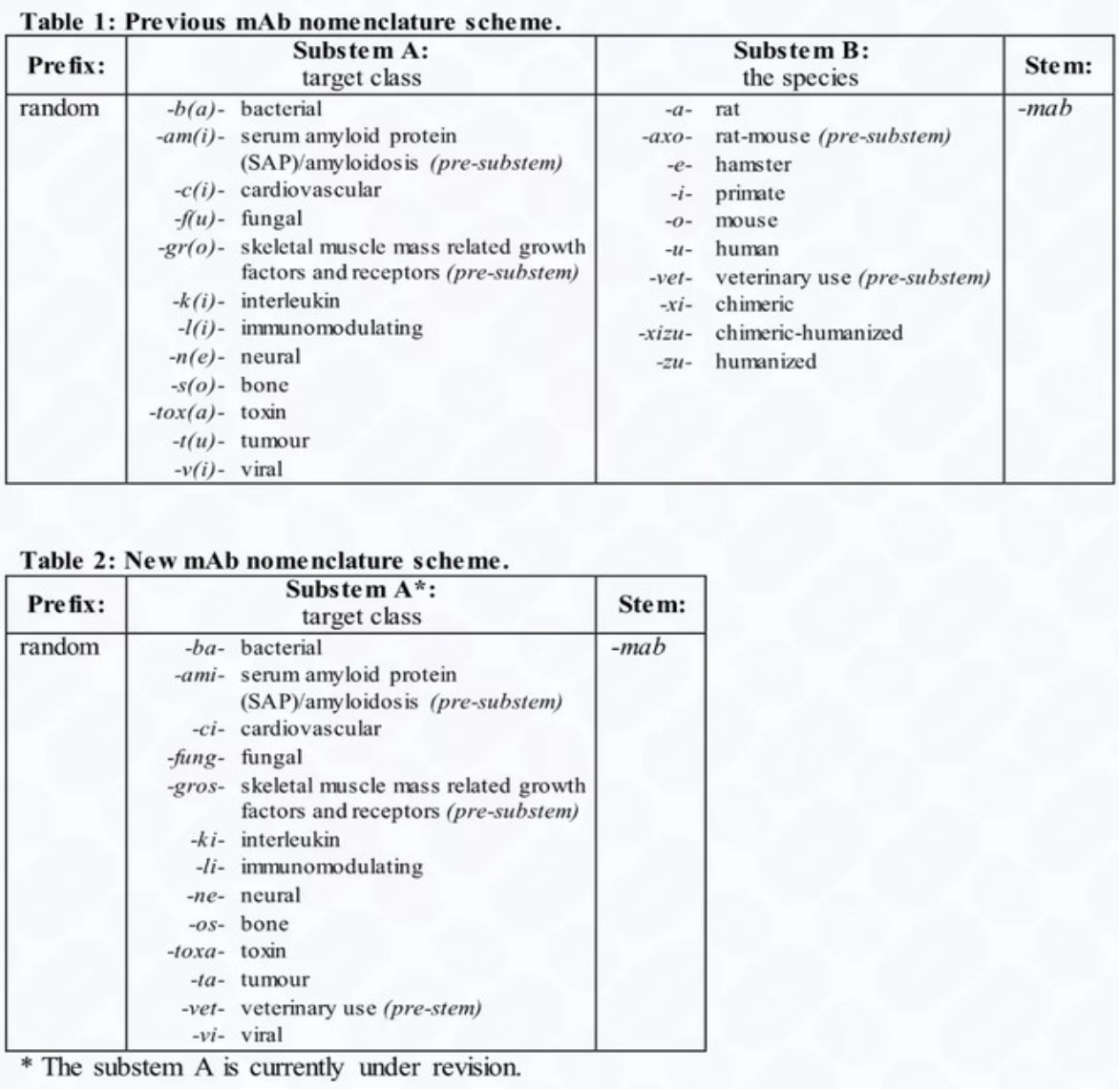
单抗药命名有三部分组成,第一部分是公司命名,第二部分为亚词干和靶标词干,第三部分为主词干Mab。其中第二部分中的亚词干在17年新版中已经取消,但由于有很多药物已经上市,沿用原命名方式,因而在这边我们也一并解读。
第一部分由于是公司的命名,这个根据每家公司自己的命名喜好而来,无规律可言。
第二部分中亚词干用如下符号分别代表不同的动物来源:
1.“-O-”为鼠源性单抗;
2.“-i-”为灵长类或除人以外的其他动物来源的单抗;
3.“-xi-”代表嵌合单抗;
4.“-ZU-”代表人源化单抗;
5.“-XiZU-”代表嵌合/人源化杂交或大鼠/ 小鼠杂交单抗;
6“-U-”代表全部组分均为人的单抗,即人源性(人)单抗.
第二部分中靶标词干即说明单抗药物的作用位点。从09年开始采用新的和简化的靶标亚词干书写法,只由“辅音+ 元音”两个字母组成。如果抗体来源亚词干的第一个字母为辅音,还可省去元音字母,只用一个辅音字母。例如靶标为免疫系统的人抗体, 旧的写法是“ -limumab",新的写法是“ -lumab”。但是,某些旧的写法还保留,例如靶标为心血管系统的嵌合抗体,还沿用“-ciximab”
下面举几个例子来说明如何解读单抗药物英文名的含意。
1. Olaratumab是一种抗肿瘤单抗药物,药名由“olara-” + “-t-” + “-u-” + “mab ”组成,表明该药是抗肿瘤的人单抗。
2. Benralizumab是一种治疗哮喘的单抗药物,药名由“benra-” + “-li-” + “-zu-” +“-mab”组成,提示该药是作用于免疫系统的人源化单抗。
3. Abckimab是一种常用的抗血小板凝集的单抗药物,药名由“ab-” + “-ci-” + “-xi-”+ “-mab”构成,表明该药是一种作用于循环系统的嵌合单抗药物。
4. 抗乳腺癌单抗药物 transtuzumab,药名由“trans-”+“-tu-” + “-zu-”+“-mab”组成,因此该药是一种抗肿瘤的人源化单抗。
5. Adalimumab 的靶标是 TNF-a,药名由“ada-”+“-lim-”+ “-u-” + “-mab”构成,该药是2009年以前命名的作用于免疫系统的单抗药物。
6. 君实生物的人源化PD-1抗体Toripalimab,药名由“Toripa” +“-li-” + +“-mab”,根据最新的命名规则,其中去掉了亚词干,从通用名无法判断其人源化形式。
关于亚词干的取消,WHO INN在2017年5月的文件解释中表述:考虑到抗体通用名较长,且亚词干B会带来免疫原性强弱的暗示,而临床证明实际上免疫原性与人源化程度并不直接相关,为避免带来错误的商业意义的暗示,取消了亚词干。
同时随着抗体药物新品种的不断出现,如双抗,ADC等药物,命名规则也在不断跟上潮流。
如默克公司的M7824其结构为在Avelumab基础上融合TGFβRII的双功能抗体融合蛋白,可以同时阻断PD-/PD-L1和TGFβ通路。2018年5月,WHO发布了融合蛋白的命名原则。根据新的命名原则,M7824的通用名已公布,为Bintrafusp alfa。不同于Fc融合蛋白以前缀“ef-”或后缀“-cept”表示,抗体融合蛋白用后缀“-fusp”表示,同时加2个中缀表示不同的功能蛋白,如Bintrafusp中的‘-r’表示受体(TGFβRII),“-a”表示抗体(PD-L1抗体avelumab)。
参考资料
1. World Intellectual Property Organization. About the nice classification. [accessed 2022 April 27].
2. World Intellectual Property Organization. Class 5 of nice classification. [accessed 2022 April 27].
3. The use of stems in the selection of International Nonproprietary Names (INN) for pharmaceutical substances. Geneva (Switzerland): World Health Organization; 2018. [accessed 2022 April 27].
4. International Nonproprietary Names (INN) for biological and biotechnological substances (a review). Geneva (Switzerland): World Health Organization; 2019. [accessed 2022 April 27].
5. Robertson JS, Loizides U, Adisa A, López de la Rica Manjavacas A, Rodilla V, Strnadova C, Weisser K, Balocco R.. International Nonproprietary Names (INN) for novel vaccine substances: a matter of safety. Vaccine. 2022;40(1):21–9. doi: 10.1016/j.vaccine.2021.11.054. PMID: 34844820
6. Köhler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature. 1975;256(5517):495–97. doi: 10.1038/256495a0.
7. Ecker DM, Jones SD, Levine HL. The therapeutic monoclonal antibody market. MAbs. 2015;7(1):9–14. doi: 10.4161/19420862.2015.989042. PMID: 25529996